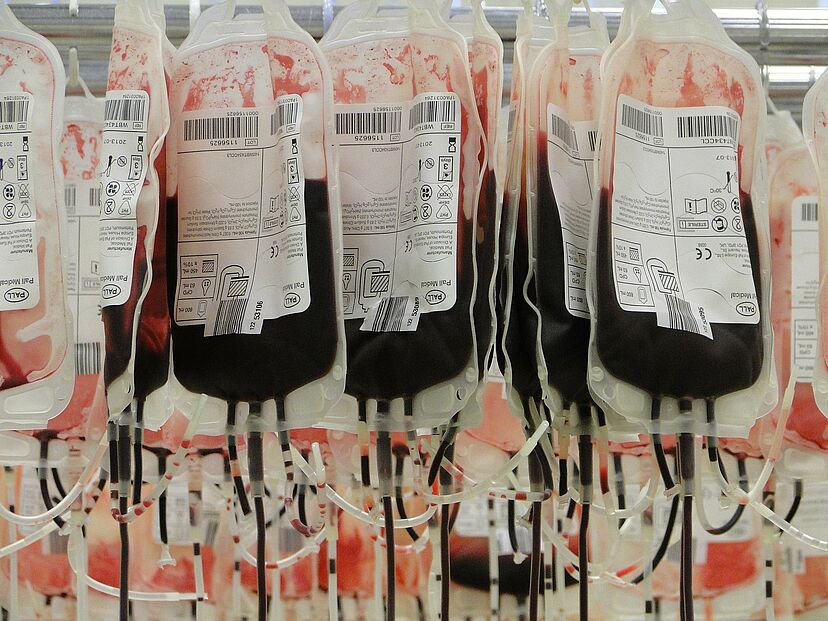
Die Antikörper, die der Körper von geheilten Infizierten produziert hat, werden mit der Blutspende gewonnen und einem Kranken, oder zur Vorbeugung auch einem Gesunden, übertragen. Der Vorteil dieser Behandlung gegenüber einer normalen «aktiven» Impfung ist, dass sie schneller wirkt. Zudem ist bekanntermassen noch kein Impfstoff gegen SARS-CoV-2 marktreif. Bei der aktiven Impfung benötigt der Körper einige Tage, um die Antikörper zu entwickeln. Zudem variiert die Zeitspanne je nach Impfstoffempfänger. Daher ist die passive Antikörperverabreichung das einzige Mittel, um eine sofortige Immunität zu verleihen. Im angesehenen Journal of Clinical Investigation rieten jüngst New Yorker Mediziner des Albert Einstein College of Medicine trotz historisch durchaus widersprüchlicher Ergebnisse dringend dazu, mit den Vorbereitungen für den Noteinsatz der Antikörper-Therapie schnellstmöglich zu beginnen.
Das Serum, das diese virusneutralisierenden Antikörper enthält, kann auch prophylaktisch verabreicht werden, um eine Infektion in Fällen mit hohem Risiko zu verhindern, beispielsweise bei schutzbedürftigen Personen mit Grunderkrankungen, Gesundheitsdienstleistern und Personen mit Exposition gegenüber bestätigten Fällen von COVID-19. Zusätzlich könnte Rekonvaleszenzserum möglicherweise bei Personen mit klinischer Erkrankung verwendet werden, um Symptome und Mortalität zu verringern. Die genaue Wirksamkeit dieser Ansätze ist nicht bekannt, aber historische Erfahrungen legen nahe, dass Rekonvaleszenzseren bei der Vorbeugung von Krankheiten wirksamer sein können als bei der Behandlung etablierter Krankheiten. Die Behandlung schützt nicht sehr lange, schätzungsweise maximal drei Monate.
Historische Belege
Während der Spanischen Grippe waren Hunderte Schwerstkranke mit dem Blut genesener Patienten behandelt worden: Durch Transfusion des Blutserums mit den Antikörpern (Immunglobulinen) wurde die Sterblichkeit nachweislich gesenkt. Mittlerweile hat sich die passive Immunisierung weiter entwickelt. Gegen Masern, Polio, Mumps, Schweine- und Vogelgrippe, auch gegen Ebolaviren wurde Blutserum bereits erfolgreich eingesetzt.
Im einundzwanzigsten Jahrhundert gab es zwei weitere Epidemien mit Coronaviren, die mit einer hohen Mortalität in Verbindung gebracht wurden, SARS1 im Jahr 2003 und das Middle East Respiratory Syndrome (MERS) im Jahr 2012. Die SARS1-Epidemie wurde eingedämmt, aber MERS wurde im Nahen Osten endemisch und löste einen sekundären großen Ausbruch in Südkorea aus. Bei beiden Ausbrüchen führten die hohe Mortalität und das Fehlen wirksamer Therapien zur Verwendung von Rekonvaleszenzserum. Die größte Studie betraf die Behandlung von 80 Patienten mit SARS in Hongkong. Patienten, die vor dem 14. Tag behandelt wurden, hatten eine verbesserte Prognose, die durch die Entlassung aus dem Krankenhaus vor dem 22. Tag belegt wurde. Diese Ergebnisse stimmen mit der Annahme übereinstimmt, dass eine frühere Verabreichung zu wirksameren Ergebnissen führt.
Aktuelle Studie aus China
Es gibt Berichte, dass Rekonvaleszenzserum während des aktuellen Ausbruchs in China zur Therapie von Patienten mit COVID-19 verwendet wurde. Obwohl nur wenige Details über die Epidemie in China verfügbar sind und veröffentlichte Studien eine kleine Anzahl von Patienten betrafen, deuten die verfügbaren Informationen darauf hin, dass die Verabreichung von Rekonvaleszenzserum die Viruslast verringerte und zu keinen Nebenwirkunen führte.
In Jama, dem Fachblatt der großen amerikanischen Medizinervereinigung, sind zum ersten Mal die Daten von einer durch internationale Experten begutachteten chinesischen Publikation mit einem begleitenden Kommentar zweier Transfusionsspezialisten erschienen. Ausführlich beschreiben die Ärzte aus dem Third People's Hospital in Shenzhen, wie sie ab Ende Januar ihren mit Spenderblut behandelten schwerstkranken Intensivpatienten das Leben retten konnten.
Alle fünf Patienten (Altersgruppe 36-65 Jahre; zwei Frauen) erhielten zum Zeitpunkt der Behandlung eine künstliche Beatmung und alle hatten antivirale Mittel und Methylprednisolon erhalten. Nach der Serumtransfusion normalisierte sich die Körpertemperatur innerhalb von drei Tagen bei vier von fünf Patienten, der SOFA-Score nahm ab und auch der Sauerstoffgehalt im Blut, ausgedrückt im Pao2 / Fio2 Wert stieg innerhalb von 12 Tagen an. Die Viruslast nahm ebenfalls ab und wurde innerhalb von 12 Tagen nach der Transfusion negativ. SARS-CoV-2-spezifische ELISA- und neutralisierende Antikörpertiter nahmen nach der Transfusion zu. Das akute Atemnotssyndrom (ARDS) löste sich bei vier Patienten 12 Tage nach der Transfusion auf, und drei Patienten konnten innerhalb von zwei Wochen nach der Behandlung von der künstlichen Beatmung befreit werden. Von den fünf Patienten wurden drei aus dem Krankenhaus entlassen und 2 sind nach der Transfusion in einem stabilen Zustand.
Die begrenzte Stichprobengröße, das Fehlen einer Kontrollgruppe und das begrenzte Studiendesign schließen eine endgültige Aussage über die potenzielle Wirksamkeit dieser Behandlung aus, allerdings sollten die Ergebnisse Mut machen, das Thema in weiteren klinischen Studien zu verfolgen.
Risiken und Nutzen
Die Risiken einer passiven Verabreichung von Rekonvaleszenzseren lassen sich in zwei Kategorien einteilen: bekannte und theoretische. Bekannte Risiken sind solche, die mit der Übertragung von Blutsubstanzen verbunden sind, einschließlich einer versehentlichen Infektion mit einem anderen Erreger einer Infektionskrankheit und Reaktionen auf Serumbestandteile, einschließlich immunologischer Reaktionen wie Serumkrankheit. Mit modernen Blutbankentechniken, die nach durch Blut übertragenen Krankheitserregern suchen und der Blutgruppe von Spendern und Empfängern entsprechen, ist das Risiko, versehentlich bekannte Infektionserreger zu übertragen oder Transfusionsreaktionen auszulösen, relativ gering. Ein gewisses Risiko beseht bei Blutransfusion allerdings für eine transfusionsbedingte akute Lungenverletzung (TRALI).
Das theoretische Risiko beinhaltet das Phänomen der antikörperabhängigen Verstärkung der Infektion (ADE). ADE kann bei mehreren Viruserkrankungen auftreten und beinhaltet eine Verstärkung der Krankheit in Gegenwart bestimmter Antikörper. Für Coronaviren wurden verschiedene Mechanismen für ADE beschrieben, und es besteht die Gefahr, dass Antikörper gegen einen Coronavirus-Typ die Infektion mit einem anderen Virusstamm verstärken könnten. Allerdings legen verfügbaren Beweise aus der Verwendung von Rekonvaleszenzseren bei Patienten mit SARS1 und MERS und anekdotische Beweise aus der Verwendung bei 245 Patienten mit COVID-19 nahe, dass die Behandlung relativ sicher ist. In Rekonvaleszenz-Serumversuchen ist jedoch generell Vorsicht und Wachsamkeit gefordert, um Hinweise auf eine verstärkte Infektion zu identifizieren.
Ein weiteres theoretisches Risiko besteht darin, dass die Verabreichung von Antikörpern an diejenigen, die SARS-CoV-2 ausgesetzt sind, die Immunantwort abschwächt und diese Personen für eine nachfolgende Reinfektion anfällig macht. In diesem Zusammenhang wurde berichtet, dass die passive Antikörperverabreichung vor der Impfung mit dem Respiratory Syncytial Virus die humorale, aber nicht die zelluläre Immunität abschwächt. Dieses Problem könnte im Rahmen einer klinischen Studie untersucht werden, indem die Immunantworten bei exponierten und mit Rekonvaleszenzseren behandelten Personen gemessen werden, um Krankheiten vorzubeugen. Wenn sich das Risiko als real herausstellte, könnten diese Personen gegen COVID-19 geimpft werden, sobald ein Impfstoff verfügbar wird.
Die New Yorker Mediziner kommen auf Basis der vorliegenden historischen und aktuellen Daten und der hohen Mortalität von COVID-19, insbesondere bei älteren und schutzbedürftigen Personen, zu der Schlussfolgerung, dass die Vorteile einer passiven Immunisierung bei Personen mit hohem Risiko die möglichen Nachteile einer Behandlung übertreffen.
Quellen:
1. The Journal of Clinical Investigation: «The convalescent sera option for containing COVID-19», Arturo Casadevall and Liise-anne Pirofski; (https://www.jci.org/articles/view/138003)
2. Jama: «Treatment of 5 Critically Ill Patients With COVID-19 With Convalescent Plasma»; Chenguang Shen, PhD; Zhaoqin Wang, PhD; Fang Zhao, PhD; et al; https://jamanetwork.com/journals/jama/fullarticle/2763983?guestAccessKey=16577a45-35ec-456b-9ad6-29f015cb11a5&utm_source=silverchair&utm_medium=email&utm_campaign=article_alert-jama&utm_content=olf&utm_term=032720